-

FDA 2016年第一季度批准新药数据分析
据FDA网站信息分析,随着快速审评通道、突破疗法、优先审核、加速审批四个快速审批途径的推进,孤儿药和生物抗体类备受重视。但是面对已批上市新药不良反应频频报警的形势,FDA药品评价和研究中心在对新药审评过程进行了创新的前提下也更加严谨。据统计显示,2016年一季度美国FDA批准了14个新生物制剂和化学药物上市,抗丙型肝炎病毒药物、抗HIV病毒药物、控制和预防血友病出血的药物和作用于神经系统的药物仍是重点。据FDA网站信息分析,随着快速审评通道、突破疗法、优先审核、加速审批四个快速审批途径的推进,孤
2016-04-09 -

吉利德抗击HIV药物管线纵览
近期,吉利德发布特大喜讯,旗下基于TAF (tenofovir alafenamide fumarate,富马酸替诺福韦艾拉酚胺)开发的二合一抗HIV组合物Descovy(emtricitabine/tenofovir alafenamide,恩曲他滨/富马酸替诺福韦艾拉酚胺,200/10mg和200/25mg)获得FDA积极意见,有望批准联合其他HIV抗逆转录病毒药物,用于12岁及以上儿童及成人HIV感染者的治疗。消息曝出当日,吉利德股价上涨0.13%,直逼95.0美元高位,收盘94.24美元
2016-04-08 -

IMS:FDA欲废止优先审评券,快速审批走火入魔?
对于21世纪的制药业来说,他们对于FDA最大的诉求就是快速的审批。 不管FDA如何努力,大药厂都觉得新药审批的机制太慢。自从《处方药申报者付费法案》设立以来,为了加快审批,大药厂乐于支付更高的费用来支持FDA加速审批。
2016-04-07 -

肺癌重大突破!百时美PD-1免疫疗法Opdivo获欧盟批准非鳞状非小细胞肺癌
美国制药巨头百时美施贵宝(BMS)是PD-1/PD-L1免疫治疗领域的绝对霸主,其PD-1免疫疗法Opdivo在黑色素瘤、非小细胞肺癌、肾细胞癌等实体瘤领域先后斩获多个批文,令该领域其他竞争对手包括默沙东、罗氏、阿斯利康、辉瑞等制药巨头望尘莫及。最近一个月,Opdivo在欧盟监管方面更是喜讯不断。上月底,欧盟正式受理Opdivo治疗经典霍奇金淋巴瘤(cHL)的新适应症申请,标志着PD-1/PD-L1免疫疗法首次进入血液肿瘤领域。而在4.1愚人节当天,百时美免疫管线中备受业界关注的组合疗法Opdi
2016-04-07 -

药品临床试验数据最残酷核查开始,有几家能扛得住?
3月29日,国家食品药品监督管理总局(简称“总局”)下发了《总局关于印发药物临床试验数据核查工作程序(暂行)的通知》(简称“通知”),这意味着从2015年7月开始的药物临床试验数据核查收紧工作迎来了最“残酷”的高潮。为什么说它残酷?让我们逐一分析。首先,核查对数据真实完整的要求非常苛刻。根据总局官网发布的《药物临床试验数据现场核查要点》(简称“要点”),核查将对所有数据的可溯源性和真实有效性进行全方位、地毯式搜寻,确保无遗漏、无死角,并明确绝对不允许拒绝或逃避检查。这要求研究数据、检测数据、试验
2016-04-01 -
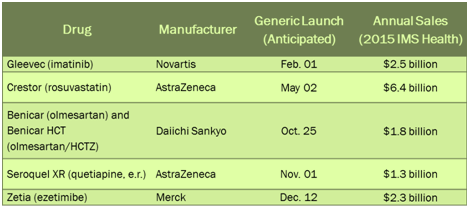
2016年重磅炸弹药物管线潜力十足
2016年有望是仿制药开始繁盛的一个大年,预计将有200亿美元流向仿制药市场。随着几种品牌药物专利保护权到期、新型生物仿制药可能得到批准、治疗癌症、糖尿病、丙型肝炎的新型疗法的出现,2016年将成为极具分量的一年,期间数种重磅药物可能会在美国批准上市。2016年有望是仿制药开始走向繁盛的一个大年,预计将有200亿美元流向仿制药市场。2月1号,印度制药公司SUN发起了诺华重磅抗癌药物格列卫 (Gleevecd)的仿制药,这将对该药2016年的销售造成很大冲击。格列卫在2001年首次被批准用于治疗费
2016-03-30 -

2016年即将上市的7个重磅炸弹药物
《财富》杂志3月25日报告了汤森路透的一项研究,认为2016年上市的新药中有7个药物有望在2020年成为重磅炸弹,而且未来年销售峰值均将超过20亿美元。NO.1 Obeticholic acid(奥贝胆酸)公司:Intercept制药/日本住友制药适应症:非酒精性脂肪性肝炎、原发性胆汁性肝硬化等慢性肝病2020销售额预测:26.2亿美元奥贝胆酸已经被证明对非酒精性脂肪性肝炎有效。非酒精性脂肪性肝炎患者数量庞大,全球患病人数大约占全球总人口的2%~3%,而且这个比例随着肥胖和胰岛素抵抗患者数量的增
2016-03-28 -

聚焦生物类似药(3):火热背后的冷思考
尽管生物类似药目前的市场规模并不算大,只有区区几十亿美元,但是却“热”得烫手。国内外许多药企都已经或打算进军生物类似药市场,世界著名仿制药公司如梯瓦(以色列)、山德士(瑞士,诺华旗下)等均加大了对生物类似药的投资力度,更有不少世界原研制药巨头如辉瑞(美国)、默沙东(美国)、安进(美国)、勃林格殷格翰(德国)等也纷纷进军生物类似药。就生物类似药火热的背后原因和驱动因素笔者三年前曾经问过“生物仿制药为什么这么火?”,答案包括: 1)日益升高的新药开发成本; 2)到期的生物药专利;以及3)市场对生物药
2016-03-27 -

聚焦生物类似药(2):生物类似药 VS. 化学仿制药
生物类似药和化学仿制药虽然都有着共同的目标—治病救人,并且都属于仿制药类别,但是两者显著不同。相比于化学仿制药,生物类似药主要有“两高”的特点:即技术门槛高、投资门槛高。一般认为生物类似药研发通常需要8-10年,比化学药仿制药3-5年要长很多。世界最大的仿制药公司之一、著名跨国药企诺华旗下的山德士认为一种典型的化学仿制药的仿制成本为2-3百万美元,而对于生物类似药而言,这一数字则高达0.75-2.5亿美元,两者相差约百倍。尽管上述研发所需的时间和金钱成本在不同的报道会有所不同,但是没有争议的是:
2016-03-27 -

聚焦生物类似药(1):何为生物类似药?
总前言笔者曾在三年前写了多篇有关生物类似药的系列文章,主要内容先后发表在《中国科学报》和《中国医药技术经济与管理》,在过去不到三年的时间里,生物类似药领域有了很大发展,尤其是中美两国在生物类似药的监管政策上都取得了很大的进展。笔者在这几年也一直关注生物类似药领域的发展,因此借美中药源和《医药经济报》联合推出“研发热点透视”专栏之际,笔者对此前的系列文章进行了全面更新和补充,以飭读者。何为生物类似药?生物类似药近年来依然是国内外制药界的热点领域,尤其在中国更是炙手可热。面对专利保护已经或即将到期的
2016-03-27 -

默沙东战胜吉利德,赢取首轮丙肝药专利权大战
本月初,默沙东和吉利德卷入丙肝药的专利诉讼案,默沙东控告吉利德侵犯了两项专利权,并索赔30亿美元。如今这场官司第一轮已经结束,默沙东获胜。若陪审团判决成立,默沙东将有权向吉利德索要其重磅丙肝药Sovaldi和Harvoni的巨额专利费。这一局官司的胜利对默沙东而言极为有利。最近默沙东丙肝药Zepatier获得FDA批准,这是继吉利德、艾伯维之后第三款上市的新型丙肝药,但是其预期销售额要远远低于吉利德的Sovaldi和Harvoni。接下来,陪审团将要权衡默沙东及其合作伙伴Ionis要向吉利德索取
2016-03-25 -

福布斯:强生、百时美新药收入占比远超其它医药巨头
当前生物制药行业发展得如火如荼,几乎每个制药商都在拼命进行新药的研发和上市。那么,究竟有多少公司是真正向市场投放了有价值的新药呢?最近一篇发表在《福布斯》杂志上的行业评论文章中,作者统计了过去5年和10年里13个制药巨头获批的新药数量,以及新药占公司年收入的百分比。结果表示百时美和强生两家公司的新药为公司的年总收入做出了重大的贡献,并且两家公司在过去五年中获批的新药数量也超过其它制药巨头。具体数字显示,两家公司的新药销售额占年总收入的50%以上。而一半以上的制药巨头在过去的10年中,其获批新药销
2016-03-24 -

【推荐】国内抗体药物研究报告
据CFDA相关老师介绍,截至2015年下半年,共有近200家药企提交抗体药物临床申请,估计国内总计有600家企业在抗体药物领域布局。考虑到数据获取的难度,以及研发水平的差异,本文仅针对已经获得受理并公开的抗体药物进行分析。
2016-03-21 -

“格拉替雷” 在多发性硬化症中会走多久?
格拉替雷是药巨头梯瓦(Teva)公司开发的治疗多发性硬化症的一线药物,2014年,在全球畅销药排位中位居第17位,销售额已连续五年超过40亿美元,位居多发性硬化药物榜首,是罕见病中重磅药物。 据了解,目前罕见病危害已经极大,并且有八成罕见病是由于基因缺陷导致,治疗手段较少,一旦出现罕见病患者,将给患者自身和家庭带来巨大的伤害。罕见病逐渐进入人们的视野,如多发性硬化症(MS)、白化病、血友病、成骨不全症、肌萎缩侧索硬化症等。
2016-03-19 -

复旦肿瘤创新药IDO 抑制剂“天价”卖出专利许可
日前,复旦大学与美国HUYA(沪亚)公司达成协议,将拥有自主知识产权的用于肿瘤免疫治疗的 IDO 抑制剂许可给美国HUYA(沪亚)公司。沪亚公司将通过里程碑付款方式向复旦大学支付6500万美金,以获得该药物在除中国大陆、香港、澳门和台湾地区以外的全球独家临床开发和市场销售的权利。这是否表明中国在药品自主研发方面已经迈入国际先进行列?是否意味着我国对进口药品的依赖度正在降低?中国药品自主研发到了什么水平复旦大学 IDO 抑制剂的研发成功,是否意味着中国现代医药的自主研发已迈入国际领先行列?答案是否
2016-03-18 -

纤维肌痛药物国内应用概览
纤维肌痛综合症(Fibromyalgia syndrome,FMS)是一种病因尚未明确的非关节性软组织风湿病,患者以慢性广泛性肌肉骨骼疼痛僵硬为特征,并伴有疲劳、焦虑、睡眠障碍、肠道应激综合症等症状。该病因临床表现复杂,且各国学者对其认识不足,直到1990年美国风湿病学会(ACR)才将该病统一命名“Fibromyalgia syndrome”,并提出统一的诊治标准,且被国际上广泛接受。ACR分类标准将FMS定义为弥漫性的慢性疼痛持续3个月以上,累及身体两侧及腰上下部,18个特殊压痛点中大于11个
2016-03-17

